Apartados
Resumen
Abstract
Introducción
Material y métodos
Resultados
Discusión
Conclusión
Referencias
1Pelayo-Olvera Sara Fernanda, 2Sánchez-Romero Tania, 2García-Bravo Mariela, 2Bañuelos-Ortiz Elise, 2Hurtado-Reyes Ignacio Carlos, 2Jiménez-Ramos Adriana, 2Ham-Armenta Cristian, 2Olivares-Mendoza Horacio. 1Médico Residente de anestesiología Hospital Ángeles Lomas. 2Médico Anestesiólogo adscrito Hospital Ángeles Lomas. CDMX.
Anestesia en México 2025;37(2): 142-147 https://doi.org/10.64221/aem-37-2-2025-010
Fecha de recepción noviembre 2024, fecha re revisión enero 2025, fecha de publicación marzo 2025.
spelayo.olvera@gmail.com
Palabras clave: Anestesia regional, paciente crítico, amputación, manejo perioperatorio.
Abstract
Keywords: Regional anesthesia, critical patient, amputation.
Introducción
Exploración física: paciente obnubilado con pobre respuesta al estímulo verbal. Signos vitales: frecuencia cardiaca (FC) 76, frecuencia respiratoria (FR) 18, tensión arterial (TA) 103/59 mm Hg, saturación periférica de oxígeno (SpO2) 87 %, con puntas nasales convencionales (PNC) a 2 L/min, soplo aórtico y mitral, no rítmico, campos pulmonares hipoventilados, gastrostomía funcional, miembros superiores con edema godete +++/++++, miembro inferior derecho con muñón bien delimitado. Pie izquierdo vendado, dedos con necrosis en distintas falanges, pulsos pedio y tibial ausentes, disminución de la temperatura. Vía aérea: sin alteraciones aparentes.
Hemoglobina (Hb) 9.13, hematocrito (Hto) 25, plaquetas 245, leucocitos 14.5, albúmina 1.23, proteínas totales 4.91, Na 130, Ca 7, tasa de filtración estimada 38.7, tiempos de coagulación TP 14.9, TPT 33.3, INR 1.23. (Imagen 1).
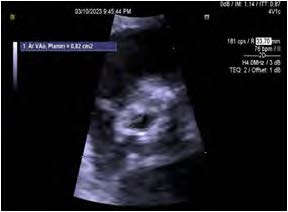
Doble lesión aórtica con predominio de estenosis de grado severo, área valvular 0.8 cm², VMAX 3.4 m/s, gradiente medio 23 mm Hg, insuficiencia de grado ligero, ventrículo izquierdo con hipertrofia concéntrica severa, FEVI 60 %, SLG -20 %. Disfunción diastólica ligera, relación E/E 9, DGL aurícula izquierda disminuida en 22 %. Insuficiencia tricuspídea y mitral ligera, PSAP 29 mm Hg. Derrame pericárdico 80 mL.
Se hace diagnóstico de osteomielitis secundaria a pie diabético y se decide amputación infracondílea en guillotina de miembro izquierdo. Se opta por realizar anestesia regional con bloqueo femoral ecoguiado. Ingresa a quirófano, obnubilado, con pobre respuesta al ambiente. Se coloca monitoreo no invasivo con los siguientes signos vitales: FC 72 lpm, FR 17 rpm, TA 137/93 mm Hg (108 mm Hg), SpO2 93 % con puntas nasales a 4 L/min, BIS 96.
Se realizó adecuada asepsia y colocación de campos estériles en región inguinal izquierda. Con ultrasonido, bajo visualización directa de arteria, vena y nervio femoral, se introduce aguja Stimuplex 100 mm hasta llegar al nervio femoral. Se administra ropivacaína al 0.375 % con lidocaína al 1 %, volumen total 20 mL. Sin incidentes.
Mantenimiento: Sedación con propofol, dosis total 20 mg; fentanilo 20 μg; fenilefrina 0.3 μg/kg/minuto. Sedación RASS -2, manteniendo ventilación espontánea con mascarilla reservorio a 10 L. Adyuvantes: Paracetamol 1 gramo, dexametasona 8 mg.
Finaliza procedimiento. Egresa paciente a recuperación hemodinámicamente estable. Signos vitales: FC 73 lpm, TA 101/52 mm Hg, FR 14 rpm, SpO2 100 % con puntas nasales (PNC) a 4 L/min. Aldrete 9/10, EVA 0, Bromage IV, náusea y vómito postoperatorio (NVPO) 0. (Imagen 2,3).
Imagen 1. Pie diabético con foco de infección activa previo a
procedimiento quirúrgico
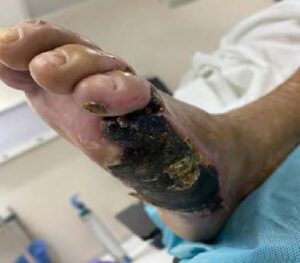
Imagen 2: Valoración ecocardiográ preoperatoria.
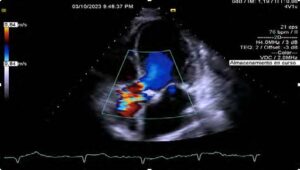
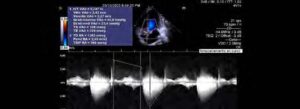
Imagen 3: Valoración ecocardiovgrá preoperatoria.
Exploración física: paciente obnubilado con pobre respuesta al estímulo verbal. Signos vitales: frecuencia cardiaca (FC) 76, frecuencia respiratoria (FR) 18, tensión arterial (TA) 103/59 mm Hg, saturación periférica de oxígeno (SpO2) 87 %, con puntas nasales convencionales (PNC) a 2 L/min, soplo aórtico y mitral, no rítmico, campos pulmonares hipoventilados, gastrostomía funcional, miembros superiores con edema godete +++/++++, miembro inferior derecho con muñón bien delimitado. Pie izquierdo vendado, dedos con necrosis en distintas falanges, pulsos pedio y tibial ausentes, disminución de la temperatura. Vía aérea: sin alteraciones aparentes.
Hemoglobina (Hb) 9.13, hematocrito (Hto) 25, plaquetas 245, leucocitos 14.5, albúmina 1.23, proteínas totales 4.91, Na 130, Ca 7, tasa de filtración estimada 38.7, tiempos de coagulación TP 14.9, TPT 33.3, INR 1.23. (Imagen 1).
Femenina de 78 años con los siguientes antecedentes de importancia: hipertensión arterial en tratamiento con candesartán 8 mg, enfermedad pulmonar obstructiva crónica Global Initiative for Chronic Obstructive Lung Disease (GOLD) 3 en manejo con oxígeno suplementario las 24 horas a 4 L/minuto, montelukast, Turbuhaler, bromuro de tiotropio, bromuro de ipratropio y salbutamol; incontinencia vesical y rectal; carcinoma epidermoide en pierna izquierda y 30 sesiones de radioterapia en la misma.
Antecedentes quirúrgicos: resección amplia de lesión cutánea en pierna izquierda en el 2022, reconstrucción de colgajo en pierna izquierda por cirugía plástica en múltiples ocasiones desde el 2022–2023. Laminectomía L3-L4, L4-L5 y descompresión en marzo 2023.
Inicia padecimiento actual hace cinco años al observar lesión en cara anterior tercio medio de la pierna izquierda. Tras tratamiento con radioterapia y múltiples sesiones por parte de cirugía plástica sin éxito, se presenta tibia al descubierto con infecciones recurrentes.
Exploración física: paciente alerta, consciente, orientada y cooperadora. Signos vitales: FC 102 lpm, FR 19 rpm, TA 125/58 mm Hg, SpO2 90 % con oxígeno suplementario. Adecuado estado de hidratación y coloración mucotegumentaria. Pupilas isocóricas y normorreflexia. Cuello sin tumoraciones ni adenomegalias palpables, sin plétora yugular. Tórax anterior con ruidos cardíacos rítmicos, S1 de intensidad constante, S2 con desdoblamiento fisiológico, diástole limpia. Tórax posterior con campos pulmonares adecuadamente ventilados, murmullo vesicular generalizado, sin estertores ni sibilancias, no se integra síndrome pleuropulmonar. Abdomen blando, depresible, no doloroso, normoperistáltico, puntos ureterales negativos. Giordano negativo. Pierna izquierda con presencia de herida longitudinal abierta con bordes bien definidos, con fibrina perilesional, visualización de hueso tibial con características necróticas, hiperemia y edema godete ++/++++.
Laboratorios: Hb 9.53, Hto 30, Leucos 5.93, Plaquetas 170, Glucosa 78.5, Urea 78.1, Cr 0.68, Au 7.1, Cl 109.2, Na 143.2, Ca 9.3, K 5.1, Mg 2.1, TP 13, TTPa 36, INR 1.10, TT 14.4.
Electrocardiograma: ritmo sinusal, frecuencia cardiaca de 90 latidos por minuto, posición vertical, transición V3, aP 60°, aQRS 60°, aT 60°, P 120 mseg, PR 160 mseg, QRS 80 mseg, QTm 360 mseg, QTc 429 mseg, alteraciones de la conducción interventricular.
Debido a mala evolución se programa amputación supracondílea de pierna izquierda. Se decide manejo con anestesia regional con sedación.
Premedicación: micronebulizaciones con bromuro de ipratropio, salbutamol y budesonida, parecoxib, hidrocortisona, un concentrado eritrocitario en preoperatorio.
Ingresa paciente a sala alerta, cooperadora. Se coloca monitoreo no invasivo con PANI, EKG, oximetría, SedLine, Rainbow, TOF, temperatura. Se obtienen los siguientes signos vitales: FC 90 lpm, TA 120/70 mm Hg, FR 18 rpm, SpO2 93 % con puntas nasales a 4 L/min.
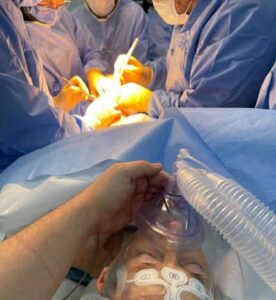
Sedación: propofol en infusión alcanzando concentración plasmática de 1 ng/mL guiado por SedLine (dosis total 200 mg), fentanilo 100 μg, midazolam 200 μg, sedación RASS -2, ventilación espontánea con oxígeno suplementario por puntas nasales a 4 L/min. (Imagen 4, 5).
Se realiza bloqueo de nervio femoral bajo control ultrasonográfico. Se coloca a paciente en supinación, se realiza adecuada asepsia y colocación de campos estériles en región inguinal y muslos izquierdo. Con ultrasonido, bajo visualización directa de arteria, vena y nervio femoral, se introduce aguja Stimuplex 100 mm. Se infiltra lidocaína 2 % (100 mg) con ropivacaína 0.4 % (75 mg) en zona de nervio femoral.
Se continúa con bloqueo de nervio ciático con abordaje anterior. Se realiza visualización de vasos femorales profundos y de fémur. Se coloca con aguja Stimuplex 100 mm bajo control ultrasonográfico el bloqueo con lidocaína 2 % (60 mg) con ropivacaína 0.4 % (75 mg). Se realiza procedimiento sin incidentes.
Adyuvantes administrados: cerebrolisina, citicolina, ceftriaxona, paracetamol, clonixilato de lisina, ondansetrón, tramadol.
Al finalizar procedimiento quirúrgico pasa paciente al área de recuperación alerta, cooperadora, ENA 0, NVPO 0, Aldrete 9/10, Ramsay II.
Imagen 4: Visualización directa del nervio femoral
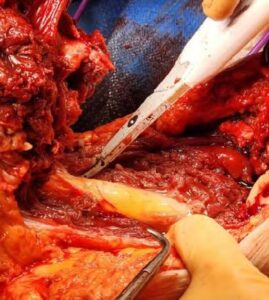
Imagen 5 : Sedación con propofol guiada por SedLine
Ante este tipo de escenarios, los pacientes presentan poca tolerancia a la inhibición del estado simpático con la consecuente hipotensión y disminución de la presión de perfusión coronaria. El paciente mantiene un estado de anticoagulación, por lo que una anestesia neuroaxial queda descartada por parte del equipo y se opta por un bloqueo femoral junto con sedación con propofol, logrando los menores cambios hemodinámicos y manteniendo un nivel de analgesia adecuado (9). Se usó fenilefrina como vasopresor auxiliar ya que, al ser un alfa agonista puro, aumenta las resistencias periféricas así como la precarga sin aumentar la frecuencia cardiaca, por lo que es uno de los vasopresores de elección para el manejo de hipotensión en pacientes con estenosis aórtica (10).
En el segundo caso se presenta un paciente con enfermedad pulmonar obstructiva crónica (EPOC) moderada-severa con dependencia de oxígeno las 24 horas del día. Aproximadamente 384 millones de personas en el mundo padecen de esta enfermedad (11) y, de acuerdo a la Organización Mundial de la Salud, en el 2019 fue la tercera causa de muerte en el mundo (12) y está asociada con el aumento de complicaciones pulmonares perioperatorias (CPP), tales como infecciones pulmonares, atelectasias, limitación ventilatoria, falla respiratoria y reintubación postoperatoria (13-14).
En la actualidad no existe un consenso o guía internacional de manejo anestésico en estos pacientes, sin embargo, se busca individualizar los casos, analizando la estrategia que brinde mayor beneficio perioperatorio. Jia-Jia Yu publicó en el 2023 un reporte de caso en donde se utilizó una anestesia neuroaxial junto con sedación con remimazolam en un paciente con EPOC severo para una resección de masa inguinal sin incidentes (15). En México no contamos con remimazolam, por lo que se optó solo por el uso de propofol guiado por SedLine, llevando la anestesia y la analgesia postoperatoria con el bloqueo femoral y ciático.
Referencias:
2. Ottokar Stundner, SGM. Regional Anesthesia and Analgesia in Critically Ill Patients: A Systematic Review. *Regional Anesthesia and Pain Medicine.* 2012; 37(5). DOI: 10.1097/AAP.0b013e3182625f1a
3. Sebastian Schulz-Stübner, André Boezaart, J. Steven Hata. Regional Anesthesia and Analgesia in Critically Ill Patients: A Systematic Review. *Critical Care Medicine.* 2005 June; 33(6). DOI: 10.1097/01.ccm.0000165843.39713.ae
4. S. Moliner Velázquez, R. Rubio Haro, C. De Andrés Serrano, J. De Andrés Ibáñez. Regional analgesia in postsurgical critically ill patients. *Revista Española de Anestesiología y Reanimación.* 2017 March; 64(3). DOI: 10.1016/j.redare.2017.01.003
5. Schulz-Stübner S. The critically ill patient and regional anesthesia. *Current Opinion in Anaesthesiology.* 2006; 19:538–544. DOI: 10.1097/01.aco.0000245281.07411.f7
6. Sigrun Halvorsen, et al. 2022 ESC Guidelines on cardiovascular assessment and management of patients undergoing non-cardiac surgery. *European Heart Journal.* 2022; 43. DOI: 10.1093/eurheartj/ehac270
7. Sorin V. Pislaru, Martin Abel, Hartzell V. Schaff, Patricia A. Pellikka. Aortic Stenosis and Non-Cardiac Surgery: Managing the Risk. *Current Problems in Cardiology.* 2015 November; 40(11). DOI: 10.1016/j.cpcardiol.2015.06.003
8. Stephanie K. Whitener, Loren R. Francis, Jeffrey D. McMurray, George B. Whitener. Asymptomatic Severe Aortic Stenosis and Noncardiac Surgery. *Seminars in Cardiothoracic and Vascular Anesthesia.* 2021 March; 25(1). DOI: 10.1177/1089253220969576
9. Eric S. Schwenk, et al. Consensus Guidelines on the Use of Intravenous Ketamine Infusions for Acute Pain Management. *Regional Anesthesia and Acute Pain.* 2018 July; 43(5). DOI: 10.1097/AAP.0000000000000806
10. Christopher B. Overgaard, Vladimír Džavík. Inotropes and Vasopressors: Review of Physiology and Clinical Use in Cardiovascular Disease. *Circulation.* 2008 September; 118(10). DOI: 10.1161/CIRCULATIONAHA.107.728840
11. Hanna Sandelowsky, Ulla Møller Weinreich, Bernt B. Aarli, et al. COPD – do the right thing. *BMC Family Practice.* 2021 December; 22(244). DOI: 10.1186/s12875-021-01583-w
12. Organización Mundial de la Salud. \[Online]; 2023 \[cited 2024 October 10]. Available from: [https://www.who.int/es/news-room/fact-sheets/detail/chronic-obstructive-pulmonary-disease-(copd)](https://www.who.int/es/news-room/fact-sheets/detail/chronic-obstructive-pulmonary-disease-%28copd%29)
13. Kristin Chino, Steven Ganzberg, Kristopher Mendoza. Office-Based Sedation/General Anesthesia for COPD Patients, Part I. *Anesthesia Progress.* 2018; 65(4). DOI: 10.2344/anpr-65-04-12
14. Factors associated with postoperative pulmonary complications in patients with severe chronic obstructive pulmonary disease. *Anesthesia and Analgesia.* 1995 February; 80(2). DOI: 10.1097/00000539-199502000-00013
15. Jia-Jia Yu, Huan-Shuang Pei, Yu Meng. Successful remimazolam sedation-epidural block in an older patient with severe chronic obstructive pulmonary disease: A case report. *World Journal of Clinical Cases.* 2023 May; 11(14). DOI: 10.12998/wjcc.v11.i14.3330
