Apartados
Resumen
Abstract
Introducción
Discusión
Referencias
Cuando los Niños Crecen, A Propósito de un Caso Con Comunicación Interventricular.
“When Children Grow Up”, Regarding a Case with Interventricular Communication.
Miguel Jovanny Jaimes-Flores1a, Rolando Enrique Matus-Pérez1b, Diógenes Alejandro Sánchez-Hernández2. 1Médico Anestesiólogo adscrito Hospital General de Zona No. 252 del IMSS Atlacomulco Estado de México. 1bMédico Anestesiólogo Hospital General de Zona con Medicina Familiar No. 41 del IMSS Huatulco Oaxaca. 2Médico Adscrito Anestesiólogo cardiovascular Hospital de Alta Especialidad, Hospital de Cardiología No. 34 del IMSS Monterrey Nuevo León.
Anestesia en México 2025; 37(3): 251–257 https://doi.org/10.64221/aem-37-3-2025-027
Fecha de recepción mayo 2025, fecha de revisión junio 2025, fecha de publicación septiembre 2025.
jovannyjj@gmail.com
Resumen
La comunicación interventricular (CIV) es la cardiopatía congénita más frecuente, si excluimos la valvulopatía aortica bicúspide, en su forma aislada. Representa aproximadamente el 20 % de las cardiopatías congénitas por lo que la CIV se clasifica según su localización: Membranosa, perimembranosa o subaórtica, supracristal el se to de salida muscular, del septo de entrada y según su tamaño en pequeñas moderadas y grandes. Los defectos pequeños suelen cerrarse de manera espontánea, mientras que los deectos grandes requieren tratamiento quirúrgico para evitar complicaciones como insuficiencia cardiaca e hipertensión portopulmonar. El propósito de este artículo es exponer el caso clínico de una paciente con comunicación interventricular con cardiopatía congénita en el adulto, tipo CIV lo cual se encontraba asintomática en clase ncio nal l ew York art Association ( sin embargo con datos ecocardiográficos de comunicación interventricular de tipo perimembranosa con cortocircuito izquierda a derecha de 4 mm de longitud, además de dilatación auricular, r lo que se comenta el caso r a considerar sesión medico quirúrgica lo cual es candidata a cirugía cardiovascular. Palabra clave: comunicación interventricular, hipertensión pulmonar, Nitroglicerina.
Abstract
Ventricular se tal defect (VSD) interventricular, is the most common congenital heart defect, excluding bicuspid aortic valve disease, in its isolated form. It accounts for approximately 20% of congenital heart defects, and is therefore classified according to location: membranous, perimembranous or subaortic, supracristal (outflow septum), muscular, inflow septum, and according to size as small, moderate, and large. Small defects usually close spontaneously, while large defects require surgical treatment to prevent complications such as heart failure and portopulmonary hypertension. The purpose of this article is to present the clinical case of a patient with ventricular septal defect with congenital heart disease in adults, type VSD, which was asymptomatic in New York Heart Association (NYHA) functional class l, however with echocardiographic data of perimembranous type ventricular septal defect with left to right shunt of 4 mm in length, in addition to atrial dilation, for which the case is discussed to consider a medical-surgical session which makes her a candidate for cardiovascular surgery. Keywords: ventricular septal defect, pulmonary hypertension, nitroglycerin.Introducción
Las cardiopatías congénitas, se presentan en 5 % de los productos en gestación de los cuales muchos de estos fallecen al nacimiento y un 40 % tiene alguna alteración cromosómica. En los últimos 10 años han ingresaron 4,544 pacientes con algún tipo de cardiopatía (1).La incidencia de las cardiopatías congénitas depende de varios factores: El medio ambiente, zona geográfica, sexo mujeres (comunicación interauricular y la persistencia del conducto arterioso), hombres (estenosis aortica y Transposición de grandes arterias), peso bajo (persistencia del conducto arterioso) (2).
La prevalencia de las cardiopatías congénitas reportadas a nivel mundial va de 2.1 a 12.3 por 1000 recién nacidos. Entre los defectos de nacimiento, la cardiopatía congénita es la principal causa de mortalidad infantil, Comunicación Interventricular (CIV) la cardiopatía más común a nivel mundial si excluimos la válvula aortica bicúspide, en su forma aislada se representa aproximadamente el 20 % de las cardiopatías congénitas, la persistencia del Conducto arterioso (PCA) la cardiopatía más común en México, Tetralogía de Fallot (TF) la cardiopatía cianógeno más común en el primer año de edad, trasposición de grandes vasos cardiopatía más común en los recién nacidos, Comunicación Interauricular (CIA) 60 % es producida por el ostium secundum (3).
Hablando de la CIV las podemos clasificar según su localización: Membranosa, perimembranosa o subaórtica, supracristal (del septo de salida), muscular, del septo de entrada y según su tamaño en pequeñas moderadas y grandes (4).
Las comunicaciones perimembranosas (70-80 %) son defectos del tabique membranoso adyacente a la válvula tricúspide que se extienden a una cantidad variable de tejido muscular circundante; el tipo más frecuente de esta comunicación se localiza inmediatamente por debajo de la válvula aórtica (5).
Los defectos musculares trabeculares (5-20 %) están rodeados por completo de tejido muscular y pueden localizarse en cualquier lugar del tabique. Las comunicaciones del tracto de salida subpulmonar (5-7 %) se localizan en el tabique interventricular inmediatamente por debajo de la válvula pulmonar. A menudo, se las denomina defectos supracristales, conoseptales, o subarteriales doblemente relacionados; suelen asociarse con prolapso de las valvas aórticas hacia la comunicación, lo que causa insuficiencia aórtica (5-6).
Las comunicaciones del tracto de entrada (5-8 %) están limitadas en la parte superior por el anillo tricúspideo y se localizan por detrás del tabique membranoso. A veces, se las denomina comunicaciones de tipo tabique auriculoventricular.
La magnitud del cortocircuito depende del tamaño de la comunicación y la resistencia corriente abajo (es decir, obstrucción del tracto de salida pulmonar y resistencia vascular pulmonar) (7).
En comunicaciones interventriculares no restrictivas, las presiones se igualan entre los ventrículos derecho e izquierdo, inicialmente existe un gran cortocircuito de izquierda a derecha con sobrecarga de volumen de los ventrículos izquierdo y derecho. Con el tiempo, el cortocircuito significativo aumenta la resistencia vascular de la arteria pulmonar, lo que a su vez agrava la sobrecarga de la presión ventricular derecha y la hipertrofia ventricular derecha. Por último, la mayor resistencia vascular pulmonar causa inversión de la dirección del cortocircuito (del ventrículo derecho al izquierdo), con el consiguiente síndrome de Eisenmenger (8-9).
Las CIV restrictivas, que son defectos más pequeños, limitan el flujo de sangre y la transmisión de alta presión a las cavidades cardíacas derechas, la presión en la arteria pulmonar es normal o mínimamente elevada. No provocan insuficiencia cardíaca, hipertensión pulmonar ni síndrome de Eisenmenger (10). Sin embargo, las CIV moderadas producen un cortocircuito de izquierda a derecha moderadamente grande, pero con presión en la arteria pulmonar normal o solo hipertensión pulmonar de leve a moderada. Las manifestaciones clínicas pueden ser mínimas o puede haber algunos síntomas de insuficiencia cardíaca debido a la circulación pulmonar excesiva (9-11). Por lo que puede desarrollar enfermedad vascular pulmonar, una complicación potencialmente letal, es mayor en pacientes de sexo femenino y en adultos mayores con defectos no tratados, el cierre quirúrgico es seguro y eficaz, si se realiza antes de los 25 años, con mejor calidad de vida normal (12).
La CIV congénita, da como resultado un hiperflujo pulmonar debido al cortocircuito de sangre. Este cortocircuito aumenta la cantidad de sangre que pasa a través de la circulación pulmonar, lo que puede resultar en un incremento del flujo sanguíneo pulmonar conllevando a una hipertensión pulmonar, produciendo remodelación vascular desfavorable, incluyendo disfunción endotelial pulmonar y aumento en el cizallamiento endotelial, lo que contribuye a la vasoconstricción y proliferación celular en el lecho vascular pulmonar, la magnitud del cortocircuito de izquierda a derecha está influenciada por el tamaño de la comunicación interauricular, lo que afecta directamente el grado de hiperflujo (13).
El manejo anestésico de los defecto interventriculares en pacientes que cursan con hipertensión pulmonar, requiere una estrategia que minimice la resistencia vascular pulmonar y a su vez no aumente la resistencia vascular sistémica, el uso de milrinonay nitroglicerina pueden ser los vasodilatadores pulmonares selectivo mejorando la hemodinámica sin causar hipotensión sistémica significativa, lo cual es crucial en el contexto de la separación de la circulación extracorpórea sin tener grandes cambios hemodinámicos (14).
Descripción del caso:
Se trata de paciente femenino de 27 años con el diagnóstico de CIV, programada de manera electiva para cierre de comunicación interventricular.Antecedentes personales no patológicos: Tabaquismo: positivo por siete años a razón de dos cajetillas al día, Alcoholismo: positivo por siete años, frecuencia semanal, a razón de 10 cervezas por ocasión. Actividad física: intensidad moderada a intensa (crossfit).
Antecedentes personales patológicos: Enfermedades crónico-degenerativas: hipertensión arterial sistémica (HAS) en seguimiento desde hace dos años y en tratamiento desde hace dos meses con amlodipino 5 mg cada 24 horas. Historia cardiovascular: soplo cardíaco diagnosticado al nacimiento y durante la infancia, sin manejo medico ni quirúrgico. Factores de riesgo cardiovascular: ninguno.
Padecimiento actual
Femenino de 27 años de edad que ingresa por seguimiento de la consulta externa de cardiología, la paciente se encuentra por cribado por soplo cardiaco, presentándose asintomática en clase funcional l, sin embargo con datos ecocardiográficos de comunicación interventricular de tipo perimembranosa con cortocircuito izquierda derecha de 4 mm de longitud con QP: QS:2.3, además, de dilatación auricular, se comenta caso para considerar sesión medico quirúrgica en vías de valorar vía de resolución de comunicación interventricular; persistiendo durante su estancia en piso asintomática, sin datos de bajo gasto.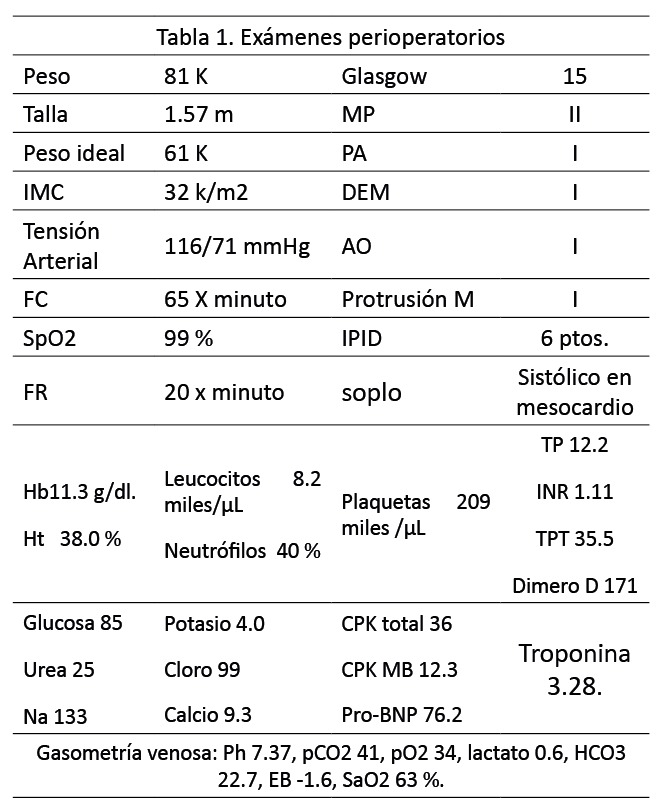
Estudios de Gabinete
Electrocardiograma normocalibrado, ritmo sinusal, Fc: 60 lpm, eje eléctrico 60 grados, onda P 80 ms, PR corto, QRS 60 ms, QTC 340 ms, sin supradesnivel, sin inversión onda T, sin necrosis, sin hipertrofia de cavidades.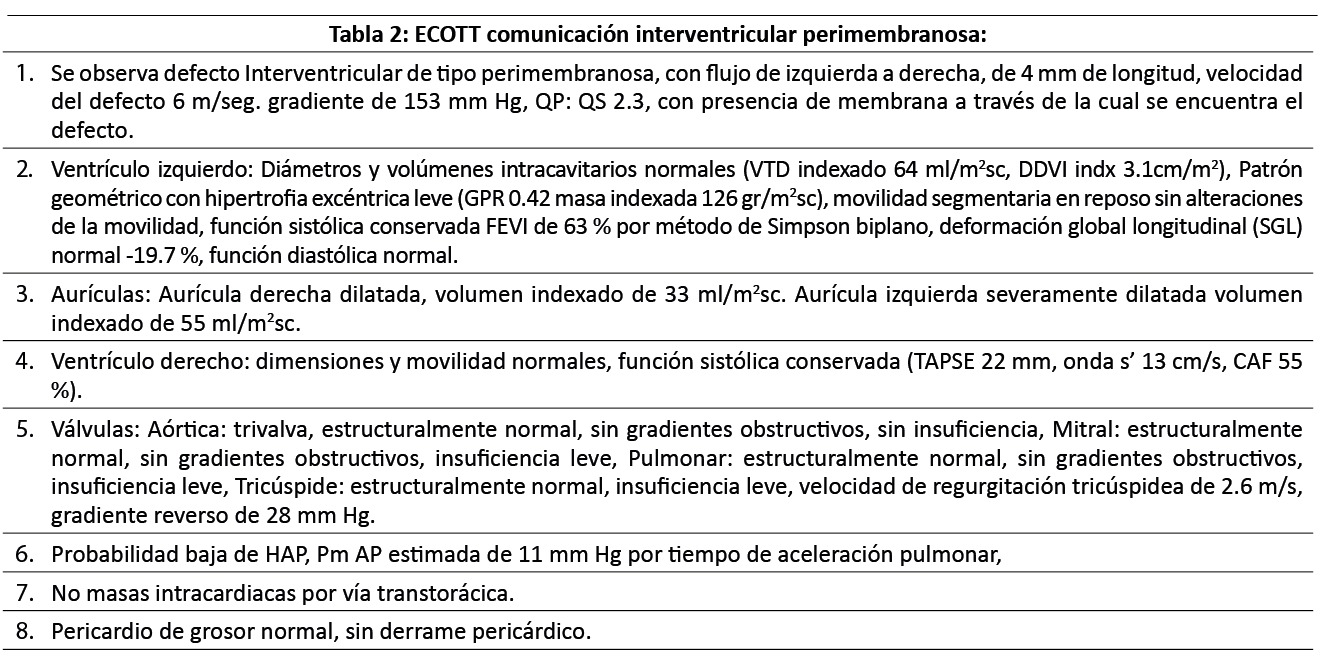
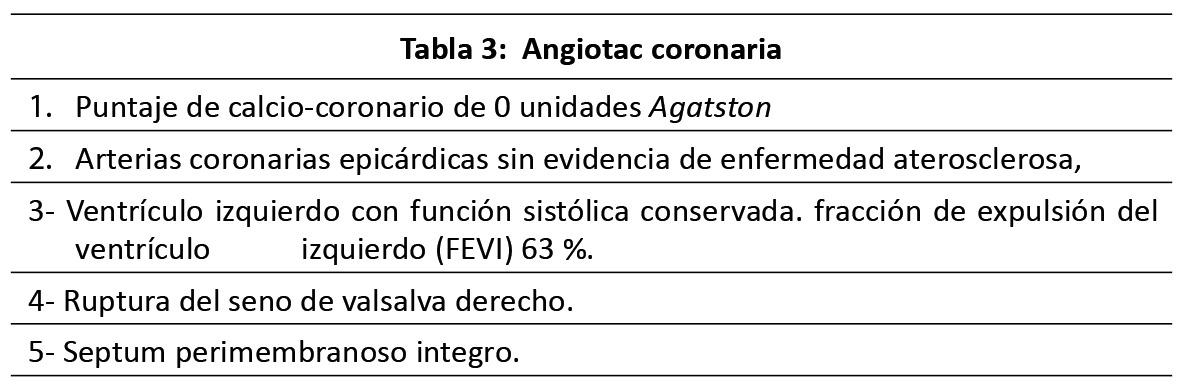
Cateterismo derecho
Catéter Swan Ganz 7.0 Fr, se puncionó arterial radial proximal, se realizo toma de gasometrías obteniendo los siguientes hallazgos: Somatometría: peso:79 kg/talla: 1.57 mts, superficie corporal: 1.8 m2; v02: 276 Ml. 02/min. frecuencia cardiaca: 65 lpm Presiones: AP: 27/18 mm hg. media: 22 mm hg. Ventrículo derecho: 35/11 mm Hg, aurícula derecha: 10 mm Hg, Presión Capilar Pulmonar: 18 mm Hg. Gasometrías: Saturación 99 %, Arteria pulmonar: 80 %, Hemoglobina: 17 g/Dl. Cálculos hemodinámicos GC: 5.3 V/min, IC: 2.85 L/min/m2SC, VL: 78 ml/latido.Rx tórax: cardiomegalia grado l, sin otras alteraciones. Valoración por cardiología: ASA II Goldman II escala de Caprini Alto. Riesgo anestésico quirúrgico: EIIIB ASA III (1.8- 5.4% de mortalidad perioperatoria, Goldman l (0.2% de complicaciones cardiacas mayores), Lee: l (0.4% de riesgo de eventos cardiacos mayores, Clasificación Destky l (0.43 % de complicaciones cardiacas mayores), Clarificación de ARISCAT 28 puntos (riesgo bajo de complicaciones pulmonares), CEPOD 2 Riesgo Cardiovascular Revisado (Intermedio), Gupta cardiaco: 1 % (riesgo intermedio de IAM perioperatorio) Jhon Hopkins: categoria 5, Caprini muy alto riesgo, APFEL 2 pts, 40 %, Riesgo de náuseas y vomito postoperatorio.
Plan
Anestesia general balanceada monitoreo invasivo. Se inicia monitoreo no invasivo Presión Arterial: 178/83 mm Hg, Presión Arterial Media 119 mm Hg, Frecuencia cardiaca 69 lpm, Frecuencia Respiratoria 18 Rpm, saturación de oxigeno 99 % temperatura 36°C, EKG con ritmo sinusal, monitoreo cerebral tipo NIRS somático y cerebral con valores de 86/75 respectivamente. Inducción anestésica: Midazolam 8 mg, Fentanilo 300 μg, Cisatracurio 10 mg. Se realizó preoxigenación y desnitrogenización con fio2 100 % HAN clase 1, durante 3 minutos, perdiendo el automatismo respiratorio se realiza laringoscopia directa, hoja MAC número 4, observando Cormack- L: Clase I, colocando Tubo Endotraqueal Numero 7.0 Murphy, se corrobora adecuada colocación mediante auscultación y línea de capnografía, fijando TET a 22 cm de comisura labial y neumotaponamiento 4 cc se conecta a circuito anestésico en ventilación mecánica controlada por volumen, Volumen Tidal : 350, Fio2 al 30 %, I: E. 1:2, FR 12, PEEP 5, Pmax: 30. Previa asepsia y antisepsia de mano derecha se coloca campo estéril se cánula línea arterial radial derecha con guía sin incidentes al primer intento.
Previa asepsia y antisepsia de cuello lado derecho se coloca campos estériles, mediante técnica de Seldinger se coloca catéter tipo CVC trilumen al primer intento.
Se coloca vía periférica en miembro torácico derecho calibre 16, sin incidentes. Se conectan monitoreo invasivo y se https://doi.org/10.64221/aem-37-3-2025-027 Anestesia en México 2025; Volumen 37 (3) : 251-257 septiembre-diciembre 256 visualiza Presión Venosa Central inicial de 4mmHg, presión arterial media 119 mm Hg, monitoreo tipo Edwards para medición de gasto cardiaco con cifras iniciales de 3.8.
Trans-Anestésico: Termodinámicamente estable: presión arterial invasiva: 70-85 mm Hg, fc 90-100 lpm, sPO2 98-100 %, PVC 4-6, gasto cardiaco por Edwards: 3.8-4.5 l/min, Mantenimiento: Sevoflurane al 2-3 vol %. (CAM 0.9 - 1) NIRS cerebral durante el procedimiento fue de 85 máximo y 74 mínimo y para el somático 79 máximo y 72 mínimo.
Adyuvantes: Dexmedetomidina a 0.3-0.5 μg/kg/hora, fentanilo total 1750 μg iv (0.009 μg/kg/min), midazolam 5 mg, cisatracurio 30 mg.
Perfusiones trans-anestésicas: Norepinefrina 0.02- 0.12 μg/kg/min, dobutamina 1 -3 μg/kg/min, Nitroglicerina: 0.5-1 μg/kg/min.
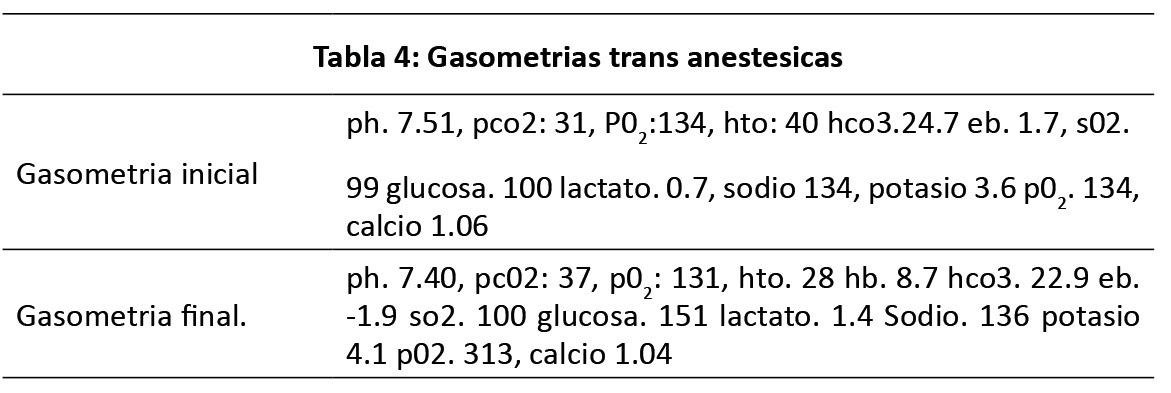
Medicación, cefuroxima 1.5 gr, heparina 25 000 UI, Protamina 300 mg, pantoprazol 40 mg, paracetamol 1 gr, ondansetron 8 mg, lisina 100 mg, morfina 2.5 gr. Se toman gasometrías arteriales para verificar el estado acido base pre y post, Cirugía cardiaca el cual se ilustran en la tabla número 4.
Discusión
La CIV es la cardiopatía congénita más frecuente, excluyendo a la válvula aórtica bicúspide, definida como un defecto septo ventricular permitiendo la comunicación de ambas estructuras, situadas dentro del grupo de cardiopatías congénitas acianógenas que cursan con aumento del flujo pumlmonar. El anestesiólogo cardiovascular debe conocer la fisiopatología de este defecto interventricular para poder tener un adecuado plan anestésico; este se debe basar en mantener una precarga y frecuencia cardiaca normal, evitando las variaciones abruptas de las resistencias vasculares sistémicas y a su vez no aumentar las resistencias vasculares pulmonares que pueden ya estar previamente afectadas si es que este defecto condiciona un hiperflujo pulmonar. La sintomatología en las CIV pequeñas, las más frecuentes, puede ser anodina, apreciándose únicamente en la exploración física un soplo pansistólico rudo, de alta frecuencia, de predominio en región paraesternal izquierda. En las CIV grandes la sintomatología es por hiperaflujo pulmonar, pudiendo originar insuficiencia cardiaca en la infancia. La intensidad del soplo es independiente del tamaño de la CIV, pudiendo ser importante en comunicaciones pequeñas y menos intenso en comunicaciones mayores. Los pacientes con sospecha de CIV deben ser evaluados mediante radiografía de tórax, que muestra, en las comunicaciones sintomáticas, cardiomegalia con hiperaflujo. El electrocardiograma muestra hipertrofia biventricular y de aurícula izquierda. La ecocardiografía y la RMN muestran la amplitud y el número de las comunicaciones. Si realizamos un cateterismo podremos ver el salto oximétrico en ventrículo derecho. Elmi-Sarabi y Cols mencionan que la administración de milrinona o nitroglicerina ha mostrado aumentar el gasto cardíaco y reducir la presión arterial pulmonar sistólica (SPAP), lo que facilita la separación de la derivación cardiopulmonar, sin aumentar la necesidad de inotrópicos intravenosos (14). En estudios comparativos, por Imam y Cols; la milrinona demostró ser efectiva en mejorar parámetros hemodinámicos como la presión arterial pulmonar sistólica y el índice de saturación de oxígeno, siendo superior a otros tratamientos. Además, se ha observado que la milrinona puede reducir la duración de la estancia hospitalaria en comparación con vasodilatadores pulmonares como sildenafil (16).
Conclusión:
En el presente caso se logró un adecuado manejo anestéhttps:// doi.org/10.64221/aem-37-3-2025-027 Anestesia en México 2025; Volumen 37 (3) : 251-257 septiembre-diciembre 257 sico cardiovascular de acuerdo a las diferentes variables hemodinámicas. Se utilizó un vasopresor para mantener presiones arteriales perfusoras en ambos contextos sin llegar a las dosis máximas de ambos, evitando los efectos no deseados, con la finalidad de tener metas terapéuticas en cirugía cardiovascular. Se brindó el manejo del dolor postoperatorio apoyado de un opioide tipo morfina con el fin de tener una extubación temprana tipo Fastrack.
Referencias
- Rubens-Figueroa J, Ceballos-Cantú Juan C, López-Ornelas Ana F, Vazquéz-Perdomo Mayela, Pablos-Hach José L. Frecuencia de cardiopatías congénitas y adquiridas en 4,544 niños. Estudio basado en ecocardiografía. Arch. Cardiol. Méx. 2021; 91(4): 407-414. DOI: 10.24875/ACM.20000166.
- De Rubens-Figueroa J, Ceballos-Cantú JC, López-Ornelas AF, Vazquéz-Perdomo M, Pablos-Hach JL. Frequency of 4,544 children with congenital and acquired heart disease. Echocardiographic study [Frecuencia de cardiopatías congénitas y adquiridas en 4,544 niños. Estudio basado en ecocardiografía]. Arch Cardiol Mex. 2021;91. DOI: 10.24875/ACM.20000166
- Tomás-Alvarado E, Ramírez-Terán ÓA. Descripción epidemiológica de niños con cardiopatías congénitas en Quintana Roo, México. Rev Mex Pediatr. 2024;91(2):64-67. DOI: 10.35366/119128.
- Hernández Morales G, Vázquez Antona CA, Muñoz Castellanos L, et al. Alteraciones aórticas asociadas a comunicación interventricular infundibular subarterial. Seguimiento ecocardiográfico [Aortic valve complications associated with subarterial infundibular ventricular septal defect. Echocardiographic follow-up]. Rev Esp Cardiol. 2002;55(9):936-42. DOI: 10.1016/s0300-8932(02)76732-8.
- Hoffman JIE, Rudolph AM. The natural history of ventricular septal defects in infancy. Am J Cardiol. 1965;16:634-9. DOI: 10.1016/0002-9149(65)90047-0.
- Castro B, Abdon. La comunicación interventricular. Revista Costarricense de Cardiología. 2000;2(1):21-26.
- Minette MS, Sahn DJ. Ventricular septal defects. Circulation. 2006;114:2190–2197. DOI: 10.1161/Circulationaha.106.618124.
- Nguyen RT, Satish P, Atkins MD, Goel SS. Rotura del tabique ventricular no diagnosticada que se presenta como insuficiencia cardíaca de nueva aparición: una complicación poco frecuente de un infarto de miocardio anterior. Methodist Debakey Cardiovasc J. 2022;18(1):113-116.
- Ghosh S, Sridhar A, Solomon N, Sivaprakasham M. Cierre transcatéter de la comunicación interventricular en el prolapso valvular aórtico y la insuficiencia aórtica. Indian Heart J. 2018;70(4):528-532. DOI: 10.1016/j.ihj.2017.11.023.
- Kenny D. Cardiología intervencionista para cardiopatías congénitas. Korean Circ J. 2018;48(5):350-364. DOI: 10.4070/kcj.2018.0064.
- Beghetti M, Tissot C. Pulmonary hypertension in congenital shunts. Rev Esp Cardiol. 2010;63(10):1179-93.
- Adatia I, Kothari SS, Feinstein JA. Hipertensión pulmonar asociada a cardiopatía congénita: enfermedad vascular pulmonar: perspectiva global. Pecho. 2010;137(6 suppl):52S-61S.
- Rychik J, Gullquist SD, Jacobs ML, Norwood WI. Análisis ecocardiográfico Doppler del flujo en el conducto arterioso de lactantes con síndrome del corazón izquierdo hipoplásico. J Am Soc Ecocardiogr. 1996;9. DOI: 10.1016/s1885-5857(10)70232-2.
- Elmi-Sarabi M, Jarry S, Couture EJ, et al. Pulmonary vasodilator response of combined inhaled epoprostenol and inhaled milrinone in cardiac surgical patients. Anesth Analg. 2023;136(2):282-94. DOI: 10.1213/ANE.0000000000006192.
- Packer M, Halperin JL, Brooks KM, Rothlauf EB, Lee WH. Terapia con nitroglicerina en el manejo de trastornos pulmonares hipertensivos. Soy J Med. 1984;76(6A):67-75.
- Imam SS, El-Farrash RA, Taha AS, Saleh GA. Milrinona versus sildenafil en el tratamiento de la hipertensión pulmonar persistente neonatal: un ensayo controlado aleatorizado. Cardiovasc Pharmacol J. 2022;80(5):746-752. DOI: 10.1097/FJC.0000000000001332.
Conflicto de intereses:
No existe conflicto de interés por parte de los autores con la Industria farmacéutica.
Apoyo financiero:
Recursos propios del autor. Ningún apoyo financiero para este trabajo que pudiera haber influido en sus resultados.
