Apartados
Resumen
Abstract
Introducción
Material y métodos
Resultados
Discusión
Conclusión
Referencias
2. Rivadeneyra-Fernández A
3. Rogel-Manzanares JD
1. Departamento de Anestesiología, Hospital General de Zona Número 14, Instituto Mexicano del Seguro Social, Hermosillo, Sonora.
2. Residente de tercer grado de la especialidad de anestesiología en el Hospital General de Zona Número 14, Instituto Mexicano del Seguro Social, Hermosillo, Sonora México.
3. Departamento de Anestesiología, Hospital General de Zona Número 15, Instituto Mexicano del Seguro Social, Hermosillo Sonora México.
Autor de correspondencia:
Dra. karla Favela Tprres
Anestesia en México 2026;38(2) https://doi.org/10.64222/aem-38-2-2026-017
Fecha de recepción 21 de enero, fecha de revisión 20 de marzo 2026, fecha de publicación mayo 2026
Correo electrónico: karlapft84@gmail.com
Objetivo: Demostrar que el ayuno con líquidos claros dos horas previas al procedimiento anestésico, versus el ayuno total, optimiza el vaciamiento gástrico en pacientes con diabetes mellitus tipo II, sometidos a endoscopia digestiva alta bajo sedación.
Materiales y Métodos: Estudio experimental, aleatorizado, analítico, prospectivo y transversal en pacientes con diabetes mellitus tipo II. Se estudiaron dos grupos de 26 pacientes cada uno: el grupo con maniobra de líquidos claros y el grupo de control. Se recolectó y midió el volumen gástrico durante el procedimiento de endoscopia. Se comparó el volumen gástrico entre grupos con la prueba U-Mann-Whitney.
Resultados: La muestra consiste en 52 mediciones: los pacientes con ayuno con líquidos claros presentaron menor volumen gástrico residual (11,9 mL, o 0,16 mL/kg) y menor incidencia (3,8 %) de residuo gástrico que los pacientes con ayuno total (31,9 mL, o 0,39 mL/kg, y 88,5 % respectivamente).
Conclusiones: El ayuno con líquidos claros optimiza el vaciamiento gástrico en pacientes con diabetes mellitus tipo II. Consideramos que es una maniobra y recomendación segura en este grupo poblacional.
Palabras Clave: Ayuno, diabetes tipo II, vaciamiento gástrico
Abstract
Objective: To demonstrate that clear-fluid fasting two hours prior to an anesthetic procedure, compared to complete fasting, optimizes gastric emptying in patients with type 2 diabetes mellitus undergoing sedated upper gastrointestinal endoscopy.
Materials and Methods: An experimental, randomized, analytical, prospective, cross-sectional study was conducted in patients with type 2 diabetes mellitus. Two groups of 26 patients each were studied: one group received the clear-fluid fasting protocol, and the other served as the control group (complete fasting). Gastric volume was collected and measured during the endoscopic procedure. Gastric volumes between groups were compared using the Mann-Whitney U test.
Results: The sample comprised 52 measurements. Patients in the clear-fluid fasting group exhibited significantly lower residual gastric volume—11.9 mL (0.16 mL/kg)—and a lower incidence (3.8%) of gastric residue compared to those in the complete fasting group, who had a residual volume of 31.9 mL (0.39 mL/kg) and an 88.5% incidence of gastric residue.
Introducción
En 1999, la ASA recomendó en adultos un ayuno de seis horas para sólidos que fueran fácilmente digeridos y un ayuno de dos horas para líquidos claros en aquellos pacientes sin antecedentes de importancia para cirugía electiva. En 2001, la iniciativa del programa Enhanced Recovery After Surgery (ERAS) —por sus siglas en inglés— estableció un protocolo de medidas preoperatorias para optimizar aspectos nutricionales y recomendó soluciones ricas en carbohidratos durante el preoperatorio. En el protocolo ERAS se implementó la pauta de líquidos claros (té de manzanilla, agua natural, gelatina de agua y bebidas carbonatadas o con electrolitos) hasta dos horas antes del procedimiento electivo en una cantidad de 200 mL como cantidad máxima. Ellos demostraron en sus estudios los beneficios de aplicar esta pauta: menor incidencia de estómago lleno, menores cambios hemodinámicos durante la cirugía, menor tiempo de recuperación y el egreso del hospital 2,3
Investigaciones sobre la fisiología de la motilidad y secreción gástrica en períodos de ayuno han demostrado que después de un período largo de ayuno se incrementa el contenido gástrico y disminuye el pH. Por el contrario, la ingesta de agua o líquidos claros dos horas antes de la anestesia disminuye el contenido gástrico y aumenta el pH por efecto de lavado y arrastre del ácido clorhídrico. El riesgo de neumonitis por broncoaspiración es mayor con un volumen gástrico >0,4 mL/kg y un pH <2,5 (4). En el paciente con diabetes mellitus tipo 2 existe la posibilidad de gastroparesia según el tiempo de evolución de la enfermedad, lo que conlleva un mayor tiempo de vaciamiento gástrico. Sin embargo, se ha detectado que el retraso es mucho mayor para sólidos que para líquidos, por lo cual las guías americanas y europeas indican que en el paciente con diabetes mellitus tipo 2 se pueden seguir las mismas indicaciones de ayuno preoperatorio que las de los adultos sin diabetes mellitus 5,7. Privar de alimentos y bebidas por horas excesivas no solo genera mayor riesgo de broncoaspiración en adultos sanos; las implicaciones metabólicas y fisiológicas son preocupantes y no debemos menospreciar que también incrementa la sensación de sed, hambre, incomodidad o ansiedad, así como alteraciones hemodinámicas durante la inducción anestésica 8. La mayoría de los estudios que han evaluado el contenido gástrico han utilizado técnicas de estimación o visualización indirecta como la aspiración con sonda orogástrica o mediante ultrasonido. La ventaja de nuestro estudio es la evaluación y medición directa después de una carga oral de líquidos claros a través de ciertos pasos que seguimos en nuestra metodología, como la aspiración primaria del contenido gástrico residual 9. Objetivo general Demostrar que el ayuno con líquidos claros 2 horas previas al procedimiento anestésico, comparado con el ayuno total, optimiza el vaciamiento gástrico en pacientes con diabetes mellitus tipo 2 sometidos a endoscopia digestiva alta bajo sedación. Objetivos específicos 1. Establecer la proporción de pacientes de cada grupo con residuo gástrico elevado (≥25 mL) como definición operacional durante la endoscopia. 2. Demostrar que la implementación de líquidos claros 2 horas antes del procedimiento reduce la presentación de hipotensión transanestésica. 3. Establecer si la pauta con líquidos claros reduce el tiempo de egreso hospitalario. 4. Medir la cifra de glucosa perioperatoria como reflejo de la resistencia a la insulina en los grupos de estudio. Material y métodos Diseño y tipo de estudio: • De acuerdo con el tipo de estudio: Ensayo clínico aleatorizado • De acuerdo con el grado de control de las variables: Experimental • De acuerdo con el objetivo: Analítico • De acuerdo con el momento en que se obtuvieron los datos: Prospectivo • De acuerdo con el número de veces que se midió la variable: Transversal Estudio realizado en el Hospital General de Zona No. 14 del IMSS, en Hermosillo, Sonora, en el servicio de endoscopias digestivas, posterior a la aprobación del Comité Local de Ética en investigación (Registro: R-2024-2601-134). Se estudiaron dos grupos: el grupo A, conformado por pacientes diabéticos tipo 2, con riesgo anestésico-quirúrgico ASA II y III, programados para endoscopia digestiva alta, debido a que se encontraban en estudio por dispepsia y síntomas de enfermedad por reflujo gastroesofágico. El grupo de intervención (A) recibió un esquema de ayuno con líquidos claros y el grupo B (grupo control) recibió un esquema de ayuno estándar de ocho horas previas al procedimiento anestésico. La asignación de grupo fue aleatorizada mediante el software Jerrydallal. 52 participantes ingresaron al estudio, de acuerdo con el cálculo del tamaño de muestra. Ambos grupos contaban con glucemias en metas y bajo tratamiento, y compartían diagnósticos similares bajo criterios de inclusión. Dos horas antes del inicio del estudio, se confirmó la arquitectura metodológica, la población basal y la maniobra de intervención, y se firmó la carta de consentimiento informado. Los pacientes asignados al grupo con líquidos claros recibieron 200 mL de gelatina de agua 2 horas previas al procedimiento; todos los pacientes programados para endoscopia acudieron a valoración preanestésica con anterioridad. En la hoja de recolección de datos se registraron signos vitales, grado de ansiedad, glucometría capilar (tres tomas: antes, durante y después del estudio), independientemente del grupo. Al cumplirse las dos horas, se ingresó al paciente para realizarse la endoscopia en posición semifowler. Se inició monitoreo tipo I y se colocaron cánulas nasales para oxígeno suplementario (2 L). Una vez logrado el plano anestésico bajo sedación grado II ASA, se inició la endoscopia por el médico endoscopista, quien observó el residuo gástrico y la calidad de imagen del estudio. Posteriormente, se realizó la aspiración del residuo y su vaciado en frasco recolector para su medición. Se documentaron, para su posterior análisis, datos como hipotensión, náuseas y vómito postoperatorio, así como el tiempo de estancia en el área de recuperación. Se realizaron pruebas de normalidad a variables numéricas y pruebas paramétricas y no paramétricas de análisis inferencial. En el análisis descriptivo, las variables categóricas o cualitativas se resumieron en frecuencia y proporción. Para el análisis inferencial y comprobación de hipótesis, se compararon medias o medianas de vaciamiento gástrico, glucosa perioperatoria, edad e índice de masa corporal (IMC) mediante prueba t de Student o U-Mann-Whitney según la distribución encontrada. La comparación de variables cualitativas (hipotensión transoperatoria, género y estado físico) fue analizada mediante prueba de Chi-cuadrado con corrección de Yates o con prueba exacta de Fisher. Se consideró una p < 0,05 como significancia estadística. Para identificar diferencias entre la prevalencia de residuo gástrico elevado (>25 mL), se aplicó la prueba de Fisher y se estimó el riesgo relativo (RR) para establecer si el ayuno con líquidos claros fue un factor protector o de riesgo, considerándose estadísticamente significativo si el intervalo de confianza era igual o superior al 95 %.
Población de estudio: Cualquier paciente sometido de manera electiva a endoscopia digestiva alta bajo sedación en el Hospital General de Zona No. 14 de Hermosillo, Sonora.
Periodo de reclutamiento: 03 de enero de 2025 al 28 de febrero de 2025.
Criterios de selección:
Grupo de pauta de ayuno preoperatorio: «Ayuno con líquidos claros» (Variable 4)
• Criterios de Inclusión:
1. Diabetes mellitus tipo 2 sin complicaciones crónicas, como retinopatía diabética.
2. Programado para endoscopia digestiva alta electiva, independientemente del motivo de la endoscopia.
3. 18 a 65 años.
4. Ambos géneros.
5. Aceptar voluntariamente participar en el estudio mediante el proceso de consentimiento informado y la firma de la carta de consentimiento informado.
6. Estado físico ASA II o III.
7. Pauta de ayuno con líquidos claros: Consumo de líquidos claros 2 horas previas al procedimiento anestésico.
• Criterios de Exclusión:
1. Paciente con prediabetes.
2. Diagnóstico de acalasia.
3. Diagnóstico asociado a hernia hiatal.
4. Tumor gástrico conocido.
5. Obstrucción intestinal.
6. Enfermedad renal crónica.
7. Uso de análogos de los receptores de GLP-1.
• Criterios de Eliminación:
1. Evidencia de falta de apego a la indicación de líquidos claros.
2. Visualización de tumor gástrico durante la endoscopia.
3. Visualización de hernia hiatal durante la endoscopia.
4. Paciente que retire su consentimiento o desee abandonar el estudio.
Grupo de pauta de ayuno preoperatorio: «Ayuno total» (Variable 4)
• Criterios de Inclusión:
1. Diabetes mellitus tipo 2 sin complicaciones crónicas, como retinopatía diabética.
2. Programado para endoscopia digestiva alta electiva, independientemente del motivo de la endoscopia.
3. 18 a 65 años.
4. Ambos géneros.
5. Aceptar voluntariamente participar en el estudio mediante el proceso de consentimiento informado y la firma de la carta de consentimiento informado.
6. Estado físico ASA II o III.
7. Pauta de ayuno total: Práctica de ayuno estándar del hospital, donde deben permanecer en ayuno con 8 o más horas para sólidos y líquidos.
• Criterios de Exclusión:
1. Paciente con prediabetes.
2. Diagnóstico de acalasia.
3. Diagnóstico asociado a hernia hiatal.
4. Tumor gástrico conocido.
5. Obstrucción intestinal.
6. Enfermedad renal crónica.
7. Uso de análogos de los receptores de GLP-1.
• Criterios de Eliminación:
1. Evidencia de falta de apego a la indicación de líquidos claros.
2. Visualización de tumor gástrico durante la endoscopia.
3. Visualización de hernia hiatal durante la endoscopia.
4. Paciente que retire su consentimiento o desee abandonar el estudio.
Cegado: Debido a la naturaleza de la intervención, no fue posible realizar el cegamiento de los participantes, ya que los pacientes asignados al grupo de líquidos claros debían ingerir de manera consciente 200 mL de gelatina de agua dos horas previas al procedimiento, lo cual implicaba necesariamente su conocimiento de la intervención. En cuanto al equipo investigador, las anestesiólogas responsables de la sedación y coordinación del estudio conocían la asignación de los pacientes para asegurar el cumplimiento del protocolo y verificar la ingesta del líquido claro previo al procedimiento. Sin embargo, se implementó un cegamiento del evaluador: el médico endoscopista encargado de la valoración y aspiración del contenido gástrico desconocía la asignación del grupo, y la cuantificación del volumen residual se realizó de forma objetiva mediante medición directa en un recipiente graduado. Asimismo, el manejo anestésico se estandarizó para todos los pacientes, independientemente del grupo asignado, con el objetivo de minimizar sesgos de desempeño y preservar la validez interna del estudio.
Control de contaminación en la medición del volumen gástrico: Con el objetivo de evitar la sobreestimación del volumen gástrico por contaminación con saliva o secreciones orofaríngeas, la medición se realizó inmediatamente tras la introducción del endoscopio, previo a la insuflación de aire o la instilación de líquidos, lo cual permitió obtener el contenido gástrico en condiciones basales. Se procuró minimizar el arrastre de secreciones mediante aspiración inicial dirigida exclusivamente al contenido intragástrico bajo visualización directa. No se realizó lavado gástrico previo a la medición, con el fin de evitar la dilución o el incremento artificial del volumen recolectado. Asimismo, la cuantificación se efectuó mediante aspiración continua hasta lograr el vaciamiento completo visible del contenido gástrico, depositándolo en un recipiente graduado para su medición objetiva. Estas medidas permitieron reducir el riesgo de contaminación y mejorar la precisión de la variable principal.
Muestra: Pacientes sometidos a endoscopia digestiva alta bajo sedación en el Hospital General de Zona No. 14 de Hermosillo, Sonora, que cumplan con los criterios de selección. Muestreo: Probabilístico, aleatorio simple, por software (http://www.000000000000jerrydallal.com/random/random_block_size_r.h).
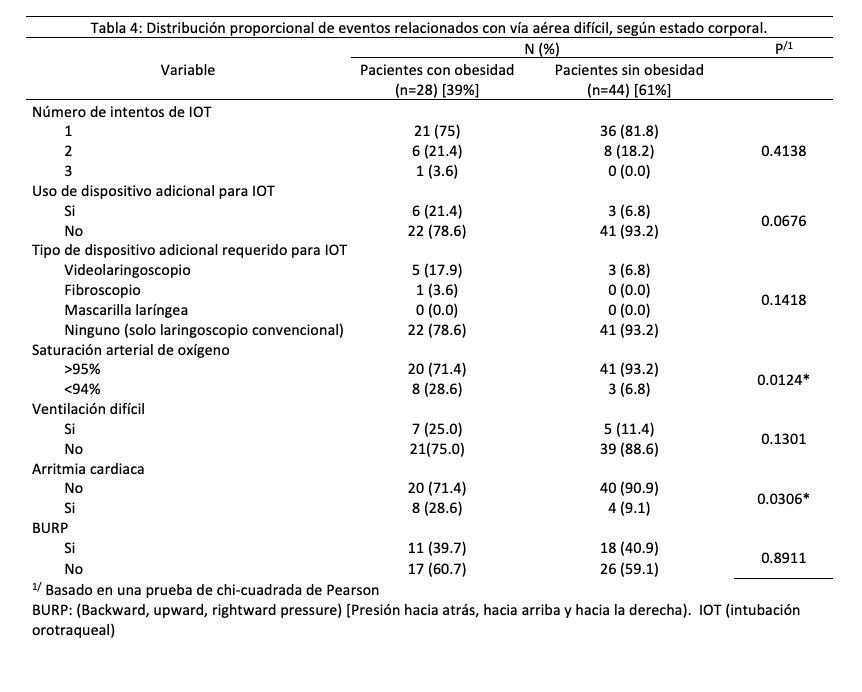
El sexo masculino representó el 53,8 % (n=28) y el sexo femenino el 46,2 % (n=24). La edad promedio fue de 55,5 años (RIQ 47-62 años). Se incluyeron pacientes con riesgo ASA II y III: el 92,3 % (n=48) correspondían a ASA II y el 7,7 % (n=4) a ASA III. La media de peso fue de 78,8 ± 9,5 kg y la de IMC fue de 27,7 ± 3,4 kg/m². La mediana de glucosa perioperatoria fue de 130 mg/dL (RIQ 111-154). Se recolectó un contenido gástrico de 23,9 mL mediante endoscopia digestiva alta (RIQ 11,8-31,9 mL), y el volumen residual medido objetivamente en un recipiente graduado fue de 0,30 mL/kg (RIQ 0,16-0,39 mL/kg). La mediana para el tiempo de egreso hospitalario fue de 30 minutos (RIQ 30-35 minutos).
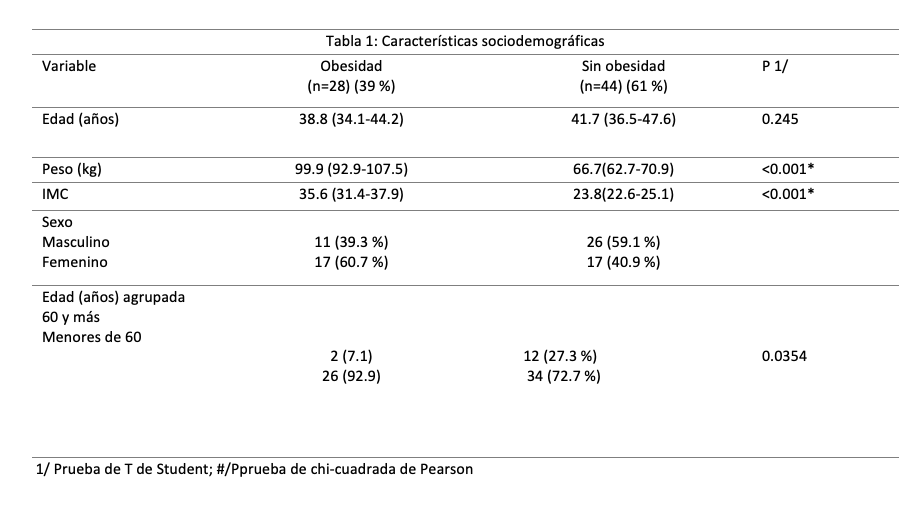
Independientemente de la escala de clasificación empleada, se observó una mayor incidencia de VAD en el grupo con obesidad en comparación con el grupo sin obesidad. Según la escala de Mallampati, el 60.7 % de los pacientes con obesidad presentaron VAD, versus 27.3 % de los pacientes sin obesidad (p=0.0048). La clasificación de Patil-Aldreti identificó VAD en el 46.4 % de los pacientes con obesidad versus el 18.2 % en el grupo II (p=0.0102). Por su parte, la escala de Bellhouse-Dore registró limitaciones anatómicas (≥1/3 de restricción) en el 46.5 % de los sujetos con obesidad, una proporción mayor al 20.5 % encontrado en los sujetos del grupo II (p=0.0455). Estas diferencias respaldan que la obesidad incrementa la frecuencia de VAD identificable mediante parámetros clínicos preoperatorios. Los detalles se despliegan en la (Tabla 2).
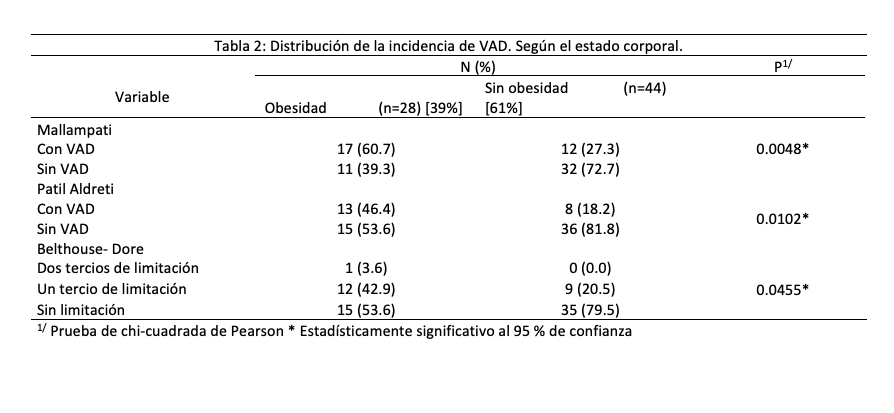
La medición ultrasonográfica de la DSE mostró diferencias significativas entre los grupos. Los pacientes con obesidad registraron una DSE promedio de 2.85 cm (IC 95 %: 2.70-3.02), superior a la observada en los pacientes sin obesidad (2.25 cm; IC 95 %: 2.13-2.38), dicha diferencia fue significativa (p<0.001). Al aplicar el punto de corte >2.5 cm propuesto por Carsetti et al. (10), el 85.7 % de los pacientes con obesidad fueron clasificados con riesgo de LD frente al 18.2 % en los pacientes sin obesidad (p<0.001). Sin embargo, la incidencia de LD confirmada intraoperatoriamente mediante la escala de Cormack-Lehane (grados III-IV) fue mayor en pacientes con obesidad (25.0 % vs. 13.6 %), aunque la diferencia no fue significativa (p=0.2207). (Tabla 3).
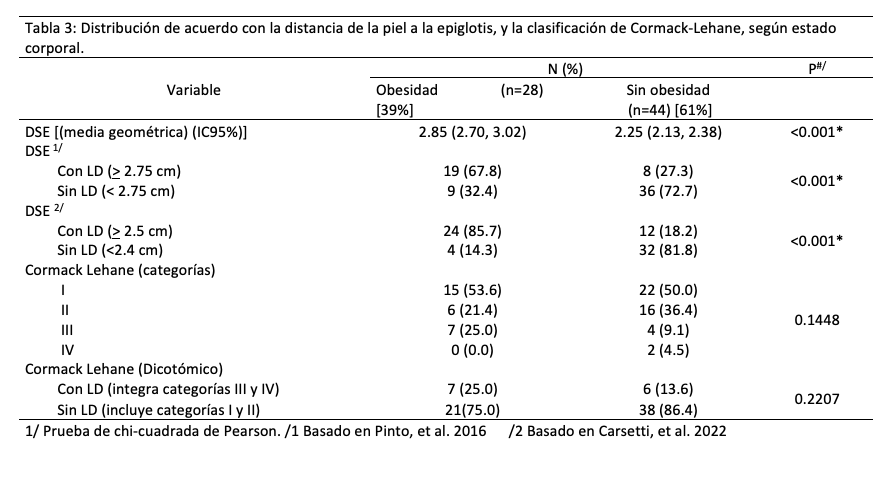
Durante el manejo anestésico, los pacientes con obesidad presentaron una incidencia mayor de eventos adversos en comparación con aquellos sin obesidad. La desaturación de oxígeno (SpO2 <94 %) se observó en el 28.6 % de los pacientes con obesidad, comparada con el 6.8 % en el grupo II (p=0.0124). Asimismo, el 28.6 % de los sujetos del grupo I desarrolló arritmias cardiacas, una proporción mayor al 9.1 % del grupo II (p=0.0306). Se observó una tendencia no significativa hacia un mayor uso de dispositivos adicionales para la intubación pacientes con obesidad (21.4 % vs. 6.8 %; p=0.0676). No se encontraron diferencias significativas entre los grupos en cuanto a la intubación esofágica, ventilación difícil, o número de intentos de intubación (Tabla 4).
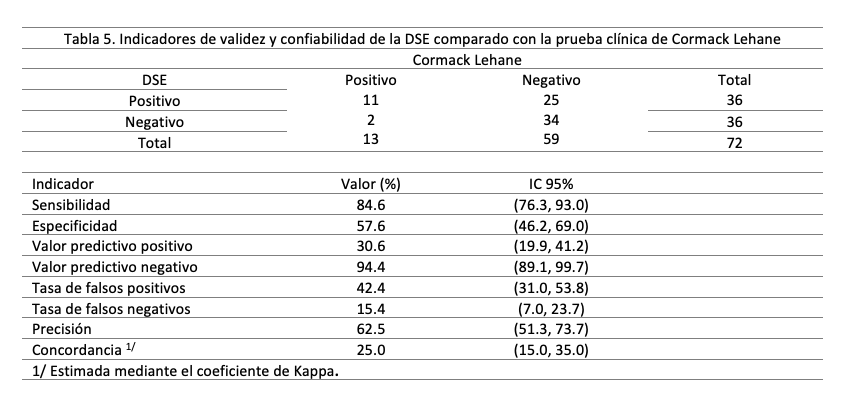
La distancia piel-epiglotis (DSE >2.5 cm) mostró una sensibilidad del 84.6 % (IC 95 %: 76.3-93.0) y una especificidad del 57.6 % (IC 95%: 46.2-69.0) para identificar LD. El valor predictivo positivo (VPP) de 30.6 % (IC 95 %: 19.9-41.2), mientras que el valor predictivo negativo (VPN) de 94.4 % (IC 95 %: 89.1-99.7). La precisión global del método fue del 62.5 %. La concordancia entre la DSE y la clasificación intraoperatoria de Cormack-Lehane –considerada como el estándar de oro– tuvo un coeficiente de Kappa de 0.25 (IC 95 %: 15.0-35.0), lo que indica que existe una concordancia limitada entre la predicción ecográfica y la evaluación directa durante la laringoscopia en este tipo de pacientes (Tabla 5).
El modelo de regresión logística (2=5.27, p=0.022) mostró que la DSE es un predictor independiente de LD, con una razón de momios = 4.16; IC 95 %: 1.15-15.0, cuadruplicando el riesgo de LD por cada aumento de 1 cm en la DSE. Por su parte, la curva ROC evidenció una capacidad discriminatoria aceptable. El punto de corte >2.5 cm mostró una alta especificidad (100 %) pero baja sensibilidad (7.69 %) para la clasificación de casos reales, lo que subraya su utilidad para descartar LD (probabilidad del 94.4 % con DSE negativa) más que para confirmarla. La curva ROC evidenció una capacidad discriminatoria moderada (AUC = 0.687), mostrando la relación entre sensibilidad y 1 − especificidad para diferentes puntos de corte de la DSE (Figura 1).
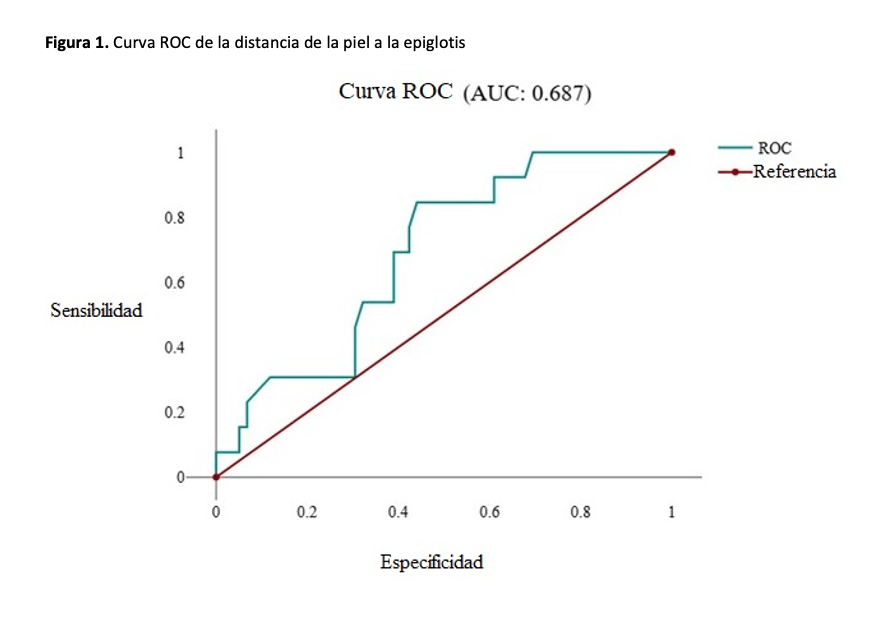
En donde:
p: Probabilidad de que ocurra laringoscopía difícil (LD = 1).
-5.26: Intercepto (constante)
1.42: Coeficiente de la variable DSE
DSE: Valor numérico de la distancia piel-epiglotis (en cm)
Por ejemplo, en un paciente con obesidad y DSE de 3.0 cm (valor superior al punto de corte >2.5 cm), el cálculo sería:
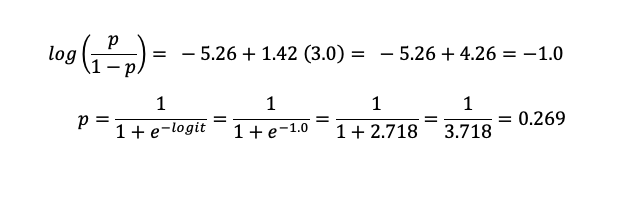
Hallazgos Principales y Consistencia con la Literatura
Los hallazgos del estudio confirman que la DSE medida por USPO posee un alto valor predictivo negativo (VPN: 94.4 %), lo que la convierte en una herramienta útil para descartar laringoscopia difícil (LD) en pacientes con obesidad. Esto implica que una DSE <2.5 cm puede descartar el riesgo de LD. Este resultado es consistente con estudios previos en poblaciones internacionales (11, 2) y respalda su utilidad como método de cribado preoperatorio.
La mayor DSE observada en pacientes con obesidad (2.85 cm vs. 2.25 cm) se asocia con una mayor incidencia de LD, atribuible a cambios anatómicos como el aumento de tejido adiposo submentoniano y pretraqueal, que profundiza la posición de la epiglotis (13,20). Además, identificamos que cada incremento de un centímetro en DSE aumenta 4.16 veces el riesgo de LD, lo que valida su valor como marcador cuantitativo independiente (14). No obstante, el punto de corte >2.5 cm procede de estudios internacionales y no ha sido validado en población mexicana. Dada la heterogeneidad morfológica de esta población (6), es necesario establecer umbrales diagnósticos locales para mejorar la precisión del método.
Limitaciones del USPO y Discrepancias con el Estándar de Oro
A pesar de su alto VPN, la especificidad moderada (57.6 %) y el bajo VPP (30.6 %) indican que la DSE no debe usarse de forma aislada para predecir VAD. Factores como la variabilidad interobservador en la medición ecográfica y la movilidad cervical intraoperatoria —no capturada en el USPO—pueden generar falsos positivos (15), lo que explica la concordancia «justa»con Cormack-Lehane (Kappa=0.25), escala que incorpora elementos dinámicos, como la apertura mandibular y la efectividad de maniobras externas (16).
Además, la discrepancia entre puntos de corte (2.5 cm vs. 2.75 cm) refleja la necesidad de estandarización. Mientras Carsetti et al. (10) proponen >2.5 cm para una mayor sensibilidad, Pinto et al. (22) sugieren >2.75 cm para mejorar la especificidad, un compromiso también observado por Udayakumar et al. (21). Nuestros hallazgos refuerzan que la DSE tiene una correlación moderada con el estándar intraoperatorio y que debe integrarse con otras herramientas clínicas para una evaluación más precisa.
Implicaciones Clínicas en el Contexto Mexicano
En México, donde 75.2 % de los adultos presentan exceso de peso y de ellos, 36.9 % obesidad (6), la evaluación preoperatoria de la VA en esta población representa un reto clínico relevante. Nuestros hallazgos respaldan la integración del USPO como herramienta complementaria, ya que
- Reduce eventos adversos: La obesidad se asoció con mayor desaturación (28.6 % vs. 6.8 %; p = 0.0124) y arritmias (28.6 % vs. 9.1 %; p = 0.0306), complicaciones prevenibles con una evaluación anticipada.
- Optimiza recursos: Una DSE >2.5 cm puede activar protocolos de VAD, reduciendo el uso emergente de dispositivos adicionales (21.4 % en obesos).
- Complementa escalas clínicas: La baja concordancia entre Mallampati y Cormack-Lehane (60.7 %) en pacientes con obesidad refuerza la necesidad de herramientas objetivas como la ecografía.
Recomendaciones para la Práctica Clínica
De acuerdo a los resultados obtenidos, se propone un algoritmo para la evaluación de VAD en casos de obesidad:
- Valoración inicial con escalas clínicas (Mallampati + Patil-Aldreti + Bellhouse Dore).
- Si el IMC ≥30: Medición de DSE por USPO.
DSE <2.5 cm: Intubación convencional.
DSE >2.5 cm: Preparar videolaringoscopio y equipo de VAD.
- En casos borderline (DSE: 2.4-2.6 cm), se recomienda combinar la medición de DSE por USPO con una evaluación dinámica de la movilidad cervical. (23-25)
Limitaciones del Estudio
Este estudio presenta algunas limitaciones. El tamaño muestral impidió un análisis estratificado por grados de obesidad, lo que impidió la evaluación de la DSE en subgrupos de mayor riesgo. La medición ecográfica fue realizada por un único operador entrenado, sin análisis de concordancia interobservador, lo que restringe la validez externa de los resultados. Además, el uso exclusivo del ecógrafo MyLab® Gamma limita la aplicabilidad en entornos con diferentes equipos, lo que resalta la necesidad de estudios multicéntricos que evalúen la reproducibilidad interequipos.
Finalmente, el punto de corte utilizado (>2.5 cm) no ha sido validado en población mexicana, lo que podría afectar la precisión diagnóstica. Futuros estudios deberían incluir múltiples operadores, diferentes dispositivos y una estratificación por grados de obesidad para fortalecer la validez externa de los hallazgos.
Declaración de Conflictos de Interés. Ninguno por declarar.
Agradecimientos
Agradezco al Hospital General del Estado de Sonora por brindarme las facilidades necesarias para la realización de este estudio. Asimismo, expreso mi profundo reconocimiento a mi equipo de colaboración, cuyo apoyo constante y compromiso fueron fundamentales para llevar a cabo esta investigación.
Referencias:
2. Altınsoy KE, Bayhan BU. Ultrasound-measured skin-to-epiglottis distance as a predictor of difficult intubation in obese patients: A prospective observational study. Journal of Clinical Medicine. 2025;14(6):2092. DOI: 10.3390/jcm14062092
3. Shaw M, Waiting J, Barraclough L, Ting K, Jeans J, Black B, et al. Airway events in obese vs non-obese elective surgical patients: A cross-sectional observational study. Anaesthesia. 2021;76(12):1585-92. DOI: 10.1111/anae.15513
4. Thota B, Jan KM, Oh MW, Moon TS. Airway management in patients with obesity. Saudi J Anaesth. 2022;16(1):76-81. DOI: 10.4103/sja.sja_351_21
5. Cook TM, Woodall N, Frerk C. Major complications of airway management in the UK: Results of the Fourth National Audit Project. Br J Anaesth. 2011;106(5):617-31. DOI: 10.1093/bja/aer058
6. Campos-Nonato I, Galván-Valencia Ó, Hernández-Barrera L, Oviedo-Solís C, Barquera S. Prevalencia de obesidad en adultos mexicanos: Ensanut 2022. Salud Publica Mex. 2023;65:S238-S247. DOI: 10.21149/14809
7. Cormack RS, Lehane J. Difficult tracheal intubation in obstetrics. Anaesthesia. 1984;39(11):1105-11. Disponible en: https://pubmed.ncbi.nlm.nih.gov/6507827/
8. Srinivasan C. Comparison of validity of airway assessment tests for predicting difficult intubation. Indian Anaesthetists Forum. 2017;18(2):63. DOI: 10.4103/jfmpc.jfmpc_1068_19
9. Casey JD, Janz DR, Russell DW, Vonderhaar DJ, Joffe AM, Dischert KM, et al. Bag-mask ventilation during tracheal intubation of critically ill adults. N Engl J Med. 2019;380(9):811-21. DOI: 10.1056/NEJMoa1812405
10. Carsetti A, Sorbello M, Adrario E, Donati A, Falcetta S. Airway ultrasound as predictor of difficult direct laryngoscopy: A systematic review. Anesth Analg. 2022;134(4):740-50. DOI: 10.1213/ANE.0000000000005839
11. Prathep S, Jitpakdee W, Woraathasin W, Oofuvong M. Predicting difficult laryngoscopy in morbidly obese Thai patients by ultrasound. BMC Anesthesiol. 2022;22(1):1-9. DOI: 10.1186/s12871-022-01685-7
12. Dabo-Trubelja A. Point-of-care ultrasound: A review of ultrasound parameters for predicting difficult airways. J Vis Exp. 2023;(194):e64648. DOI: 10.3791/64648
13. Ezri T, Szmuk P, Warters RD, Saad-Eddin H, Katz J, Hagberg C. The incidence of class “zero” airway in anesthetized patients. Anesth Analg. 2003;96(1):132-5. DOI: 10.1097/00000539-200110000-00055
14. Martínez-García A, Guerrero-Orriach JL, Pino-Gálvez MA. Ultrasonography for predicting difficult laryngoscopy. J Clin Monit Comput. 2021;35:269-77. DOI: 10.1007/s10877-020-00467-1
15. Parameswari A, Govind M, Vakamudi M. Correlation between preoperative ultrasonographic airway assessment and laryngoscopic view. J Anaesthesiol Clin Pharmacol. 2017;33(3):353-8. DOI: 10.4103/joacp.JOACP_166_17
16. Heidegger T. Management of the difficult airway. N Engl J Med. 2021;384(19):1836-47. DOI: 10.1056/NEJMra1916801
17. Roth D, Pace NL, Lee A, Hovhannisyan K, Warenits AM, Arrich J, Herkner H. Airway physical examination tests for detection of difficult airway management in apparently normal adult patients. Cochrane Database Syst Rev. 2018;5:CD008874. DOI: 10.1002/14651858.CD008874.pub2
18. Brodsky JB, Lemmens HJ, Brock-Utne JG, Vierra M, Saidman LJ. Morbid obesity and tracheal intubation. Anesth Analg. 2002;94(3):732-6. DOI: 10.1097/00000539-200203000-00047
19. Kristensen MS. Ultrasonography in the management of the airway. Acta Anaesthesiol Scand. 2011;55(10):1155-73. DOI: 10.1111/j.1399-6576.2011.02518.x
20. Wojtczak JA. Submandibular sonography: Assessment of hyomental distances and ratio, tongue size, and floor of the mouth musculature using portable sonography. J Ultrasound Med. 2012;31(4):523-8.
21. Udayakumar GS, Priya L, Narayanan V. Comparison of ultrasound parameters and clinical parameters in airway assessment for prediction of difficult laryngoscopy and intubation: An observational study. Cureus. 2023;15(7):e41392. DOI: 10.7759/cureus.41392
22. Pinto J, Cordeiro L, Pereira C, Gama R, Fernandes HL, Assunção J. Predicting difficult laryngoscopy using ultrasound measurement of distance from skin to epiglottis. J Crit Care. 2016;33:26-31.
23. Gohad R, Jain S. The use of point-of-care ultrasound (POCUS) in anesthesiology: a narrative review. Cureus. 2024;16(9):e70039. doi:10.7759/cureus.70039
24. Eissa M, Lessard G, Morales J, Rajaleelan W. Point-of-care ultrasound (PoCUS) in low- and middle-income countries. Best Pract Res Clin Anaesthesiol. 2025;[Epub ahead of print]. doi:10.1016/j.bpa.2025.11.005
25. Rominger AH, Gomez GAA, Elliott P. The implementation of a longitudinal POCUS curriculum for physicians working at rural outpatient clinics in Chiapas, Mexico. Crit Ultrasound J. 2018;10(1):19. doi:10.1186/s13089-018-0101-8
